Quelques semaines à peine après avoir reçu un traitement par thérapie génique, quatre enfants sourds de naissance ont recouvert l’audition, en Chine. CNEWS s’est entretenu avec le chercheur qui a dirigé les recherches ainsi qu’avec une autre scientifique travaillant sur un projet similaire.
C’est un espoir pour les parents dont les enfants sont atteints de surdité. En Chine, quatre enfants âgés de 2 à 6 ans, sourds de naissance, ont en effet retrouvé une audition quasi normale, après avoir reçu un traitement expérimental proposé en octobre 2022 par des chercheurs et médecins de l’hôpital ophtalmologique et ORL de l'université de Fudan (Shangaï).
Les enfants, dont la surdité avait fortement perturbé la parole, ont ainsi retrouvé «leur capacité à participer à des conversations de la vie courante après le traitement», explique Yilai Shu, médecin et chercheur qui a dirigé les investigations théoriques comme l’essai clinique.
Grâce à la fameuse «thérapie génique» – cette technique de pointe qui consiste à introduire du matériel génétique directement dans les cellules, pour pallier le manque ou le dysfonctionnement dudit matériel –, les chercheurs ont en fait pu traiter non pas tant les symptômes que leurs causes.
Une surdité d'origine génétique
Les scientifiques ont pour cela injecté, directement dans le liquide contenu dans l’oreille interne des enfants atteints de surdité DFNB9 – c’est comme ça que l’on appelle cette forme de la maladie –, une solution médicamenteuse riche en vecteurs viraux artificiellement munis d’un gène, appelé OTOF, qui manque chez ces patients. Les vecteurs viraux sont inoffensifs et sont développés pour cibler spécifiquement les cellules anormales en y déposant leur matériel génétique. Les vecteurs viraux, après leur entrée dans les cellules cibles déversent le matériel génétique souhaité et avec celui-ci seulement.
«Une équipe de chercheurs menée par le Docteur Christine Petit, à l’Institut Pasteur, a par le passé étudié des familles de personnes atteintes d'une forme héréditaire de surdité neurosensorielle, appelée "surdité autosomique récessive avec neuropathie auditive"». C'est ce que détaille le Professeur Natalie Loundon, qui dirige le centre de recherche en audiologie pédiatrique de l'hôpital Necker-Enfants malades. En 1999, poursuit-elle, l’équipe a découvert que ces familles présentaient des mutations dans un gène codant pour la protéine otoferline, localisé sur le chromosome 2 qu'ils ont appelé OTOF».
L’équipe a, dans le même temps – nous précise la chercheuse – découvert la protéine produite par OTOF, appelée otoferline, au rôle crucial dans l’audition. Les chercheurs, après avoir artificiellement reproduit la délétion de cette protéine chez des souris, pour étudier la symptomatologie qui en découle, n’ont eu de cesse de chercher un moyen de la remplacer.
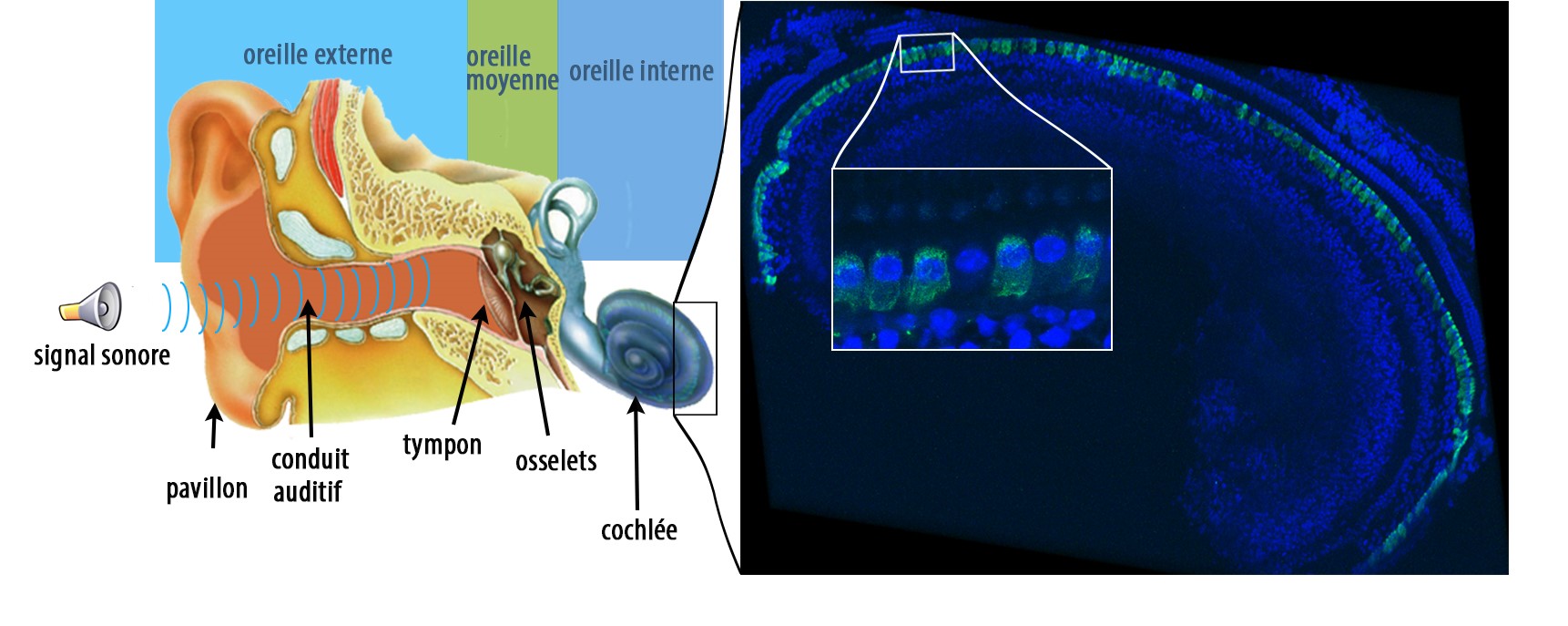
Grâce à la thérapie génique, les chercheurs sont capables de produire l'otoferline dans les cellules de la cochlée qui sont déficientes. Ici, l'otoferline, qui apparaît en vert, a pu être produite dans la majorité des cellules ciliées de souris marquées en bleu, lors de précédentes recherches (image de droite). [Institut Pasteur/Génétique et physiologie de l'audition]
Une protéine cruciale manquante
L'otoferline est en effet une protéine impliquée dans la fonction des cellules ciliées du système auditif, qui sont des cellules sensorielles qui convertissent les vibrations sonores qui parviennent à l’oreille interne en signaux électriques, qui sont ensuite transmis au cerveau.
Plus précisément, l'otoferline joue un rôle central dans un processus biologique appelé exocytose, qui consiste à libérer des neurotransmetteurs des cellules vers d’autres cellules, tel un messager. Dans le cas des cellules ciliées, l'otoferline aide à libérer le neurotransmetteur appelé glutamate, qui stimule les terminaisons des neurones auditifs et permet donc au cerveau, en somme, de recevoir un influx nerveux codant pour les sons reçus par l’oreille.
Yilai Shu ajoute : «Notre recherche visait à développer un médicament candidat [composé chimique satisfaisant les critères en termes d'efficacité et de sécurité afin d'être utilisé dans des essais cliniques sur des humains, n.d.l.r.] de thérapie génique comme stratégie étiologique pour guérir la perte auditive des patients DFNB9». Bien que la découverte se base sur de précédents travaux menés sur des souris, elle est toutefois «la première à démontrer que la thérapie génique est sure et efficace chez les patients atteints d’une perte auditive congénitale [présent à la naissance, n.d.l.r]», s’enthousiasme le chercheur. Et donc : la première à restaurer la production de l’otoferline chez des patients atteints de surdité DFNB9.
D'autres essais cliniques à venir
Si l’équipe de Yilai Shu est la première à avoir publié ses résultats, plusieurs autres essais cliniques du même type sont en cours dans le monde, notamment deux aux États-Unis et un en France. Ce dernier est mené par Natalie Loundon qui doit commencer prochainement le recrutement d’enfants.
À terme, cette révolution pourrait bien – chez les patients DFNB9 – remplacer les implants cochléaires (placés dans la cochlée, la structure interne dans laquelle se situent les cellules ciliées). «Quand l’implant fonctionne, il est certes très efficace, mais il est invasif et peut abîmer l’oreille interne», souligne Natalie Loundon. «Les patients veulent retrouver leur audition naturelle, constate le médecin. Lorsqu’il y a du bruit, quand on ne met pas l’appareil couché la nuit ou sous la douche, quand les batteries sont éteintes... il est impossible d’entendre», rappelle-t-elle.
La chercheuse et ses collègues ont bon espoir, nous explique-t-elle, d’être un jour capables de traiter la surdité d’un individu pendant pas moins de quarante ans ; et, ce, après... une seule et unique injection !
Un espoir pour traiter d'autres causes génétiques de surdité
Malgré tout, Natalie Loundon et Yilai Shu restent prudents dans leurs travaux. Ce dernier tient à souligner que «le nombre de patients [ayant bénéficié du traitement] est relativement faible et [que] le temps de suivi post injection est relativement court». «Dans le futur, poursuit-il, nous comptons étendre le nombre de patients et procéder à un suivi au long cours. Après cela, il faudra enfin un plus grand support de la part des industries et une plus grande coopération avec elles pour que cela se développe réellement, dans plusieurs années.»
L'audition est somme toute un processus complexe qui nécessite la collaboration de plusieurs organes et systèmes qui interagissent entre eux. Toute anomalie peut alors entraîner une cascade de problèmes en chaîne. Aussi, cette technique n’est pas applicable à des personnes sourdes atteintes par le vieillissement, par des produits toxiques, ou qui ont subi un traumatisme au tympan, pour ne citer que ces exemples. En outre, seuls 2 à 8% des surdités héréditaires sont liées au gène OTOF, selon les régions du globe.
Cette recherche présente néanmoins un potentiel exceptionnel pour les individus dont la maladie est liée à des causes génétiques (60% des 26 millions de personnes souffrant d’une forme congénitale). En effet, à date, explique Yilai Shu, «les scientifiques ont identifié 150 gènes [dont le dysfonctionnement] est impliqué dans la surdité». Or, ils espèrent pouvoir élaborer d’autres traitements par thérapie génique, pour chaque gène dysfonctionnel.
Parmi les gènes visés, explique Natalie Loundon : le gène GJB2, dont le dysfonctionnement perturbe la synthèse de la protéine connexine 26, et qui constitue la cause génétique la plus fréquente de surdité (35% des cas de surdité congénitales), mais pour lequel un traitement est plus difficile à élaborer. Dans le syndrome de Usher type 1 impliqué à la fois dans la surdité, la cécité et des troubles de l’équilibre, une thérapie génique pour GJB2, par exemple, permettrait de guérir les deux pathologies liées à l'oreille chez les patients atteints.
Pour l'heure, les scientifiques s'attellent, entre autres, à améliorer les connaissances des gènes présents dans les cellule de la cochlée, ainsi que leur rôle. Des résultats de travaux de recherche publiés en juin dernier, menés à l'Institut Pasteur, ont notamment montré qu'il était possible de classifier précisément les gènes impliqués dans la surdité et/ou le développement de la cochlée. De quoi favoriser l'étude plus fine de chacun d'entre eux...

![Il y a environ 26 millions de personnes atteintes de surdité congénitale dans le monde. [Photo d'illustration / grahams_photography / Unsplash].](http://static.cnews.fr/sites/default/files/directmatin/image_placeholder_rect_basic.gif)
